En nuestro estudio, si se hubiese tomado la decisión para la prueba con base en el antecedente familiar, se hubieran pasado por alto mutaciones en más de 5% de los pacientes, dijo la Dra. Nazneen Rahman, PhD, del Institute of Cancer Research, en Londres, Reino Unido. «Hemos podido realizar pruebas de BRCA durante más de 20 años, pero en general los estudios han demostrado que no tienen la eficacia que nos gustaría», dijo la Dra. Rahman en el congreso.

- inicio antes de los 40 años. La tasa de detección en esta categoría fue del 12.1%
- cáncer de mama bilateral antes de los 60 años; aquí fue del 13.6%.
- cáncer de mama triple negativo (enfermedad con negatividad para receptor a estrógeno, progesterona y HER2) a cualquier edad; en este grupo, el 10.2%
- cáncer de mama y de ovario a cualquier edad; arrojó la tasa más elevada con un 27.8% y
- cáncer de mama en un hombre. La detección en este grupo fue del 11.5%
Con el fin de confirmar estos hallazgos, el equipo de la Dra. Rahman llevó a cabo luego un estudio retrospectivo de 2.036 pacientes reclutadas por el estudio Breast and Ovarian Cancer Susceptibility (BOCS). Para cada categoría, excepto la del cáncer de mama en pacientes de género masculino, la tasa de detección de mutación fluctuó de 11,0% a 13,2%. La tasa de detección para hombres con cáncer de mama fue solo 3,2%, pero el tamaño de la muestra fue muy pequeño (31 pacientes) para determinar una tasa exacta, informó la Dra. Rahman.
Después los investigadores utilizaron dos puntuaciones de riesgo de mutación de BRCA para evaluar la precisión del antecedente familiar como un indicador. Cuando se estableció como umbral una puntuación de Manchester de un mínimo de 15, solo se identificaron 53 de las 110 (48,2%) pacientes con mutaciones. Y cuando se utilizó la puntuación de riesgo de BOADICEA (Breast and Ovarian Analysis of Disease Incidence and Carrier Estimation Algorithm) de un mínimo de 10%, solo se identificó a 42 (38,2%) de las portadoras de mutación.

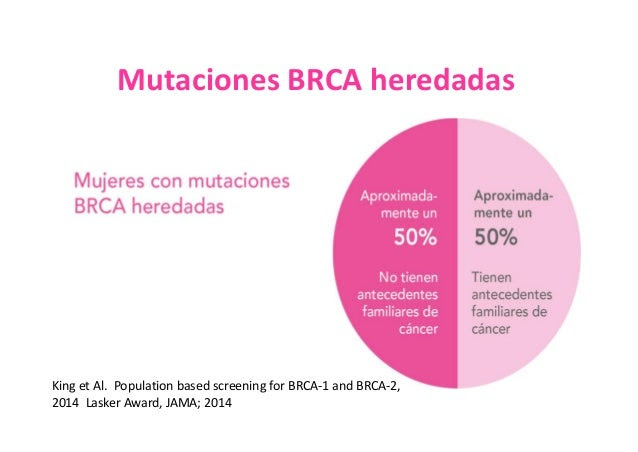
Con estos modelos de riesgo, «más de 50% de las portadoras de mutación no hubieran sido elegibles para las pruebas con base en el antecedente familiar», dijo la Dra. Rahman. Cuando las 368 pacientes con cáncer que no correspondieron a alguna de las categorías de alto riesgo pero que tenían un antecedente familiar de cáncer fueron evaluadas, la tasa de mutaciones fue de 5,4% para las pacientes con un antecedente familiar moderado y de 7,0% para aquellas con un antecedente familiar fuerte.
Lo importante de este estudio es que «una vez que se han realizado las pruebas basadas en cáncer, los criterios actuales de antecedentes familiares no son satisfactorios para predecir la probabilidad de tener una mutación», explicó la Dra. Rahman. Además, un análisis financiero demostró que el uso de las categorías de alto riesgo para identificar candidatos a pruebas genéticas, más que el antecedente familiar, ahorraría un total de 3.063.681 de libras esterlinas (4.035.480 USD) al prevenir 1.157 neoplasias malignas y 222 muertes por cáncer de mama u ovario cada año.

«Debemos reconocer que aún seguimos teniendo muchas dudas respecto a la conducta futura con las pacientes portadoras de BrCa 1 y/o 2», destaca José Luis Neyro, pues la evolución no está clara ni existe un único patrón de comportamiento de estos protoncogenes habida cuenta de la individualidad de cada mujer. Así, todavía seguimos aferrándonos a factores de riesgo epidemiológico para evaluar el riesgo (como mostramos en https://www.neyro.com/2014/06/
La estrategia ahora descrita, al parecer ofrece ventajas con respecto al antecedente familiar, como base para la elegibilidad de la prueba, dijo el Dr. Ian Campbell, PhD, del Peter MacCallum Cancer Centre, en Melbourne, Australia. «El recuerdo del antecedente familiar de las personas es notoriamente deficiente», haciendo notar que algunas personas no siempre están al tanto del cáncer en familiares en primer grado. Y otras podrían sobreestimar el riesgo debido a que un pariente femenino más distante falleció por cáncer de mama a una edad avanzada.

La implementación de un sistema basado en categorías podría reducir el uso de asesoría genética previa a la prueba, dijo Aisha Furqan, una asesora genética en el St. Agnes Medical Center, en Fresno, Estados Unidos. «Se podrían reducir algunos costos y tiempo, pero en realidad, la asesoría es invaluable para los individuos que no tienen ideas preconcebidas en torno a lo que pueden o no pueden hacer las pruebas genéticas», dijo después de la presentación. Han acudido mujeres a mi consultorio y han rechazado las pruebas genéticas después de la asesoría debido a que, en ese punto en su tratamiento o en sus vidas familiares, simplemente no estaban listas, dijo el experto. Sin embargo, podrían interesarse en otro momento, añadió.
Referencia: Rahman N, Turnbull A, George A, Strydom A, Kemp Z. Using cancer status is better, simpler and more cost-effective than family history in determining breast cancer genetic testing eligibility. Congreso anual de la American Society of Human Genetics 2017. Presentado el 18 de octubre de 2017; Orlando, Estados Unidos.
El estudio fue financiado por el Wellcome Trust y el National Institute for Health Research. La Dra. Rahman refiere prestar sus servicios en la junta de directores de AstraZeneca. El Dr. Campbell y la señorita Furqan han declarado no tener ningún conflicto de interés económico per

Un comentario sobre “El antecedente personal de cáncer es mejor que el antecedente familiar para realizar pruebas de BRCA”
Los comentarios están cerrados.